De la comida al mal funcionamiento: explorando vías moleculares, biomarcadores e intervenciones en salud cardiometabólica postprandial
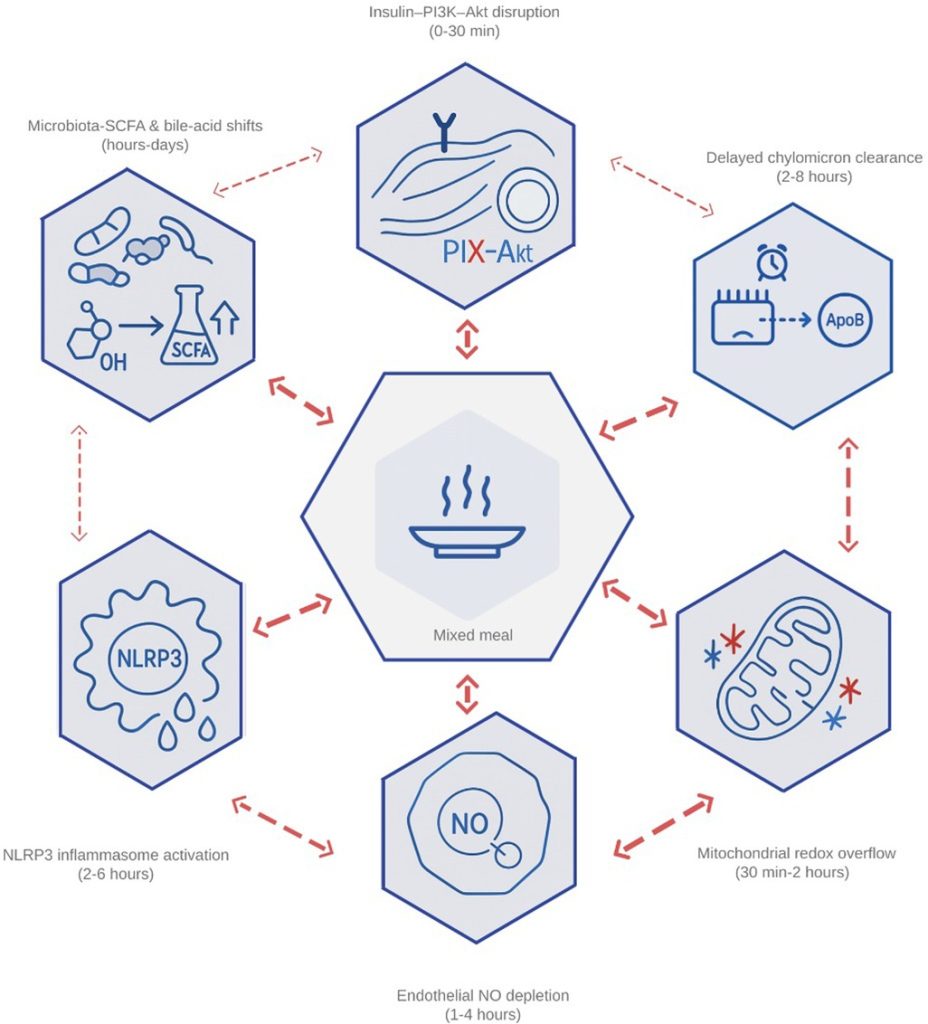
Encuentra más información en nuestro repositorio digital Las enfermedades cardiometabólicas -incluidas la diabetes tipo 2, las enfermedades cardiovasculares y la disfunción metabólica asociada a la hepatopatía esteotítica- están cada vez más impulsadas por una exposición casi continua después de las comidas a aumentos bruscos de glucosa y lípidos que a menudo se pasan por alto en las pruebas tradicionales de ayuno. Esta revisión prioriza los estudios humanos de 2020 a 2025 y utiliza trabajos anteriores solo como anclajes fundamentales; se excluyeron informes no ingleses y se citan hallazgos preclínicos únicamente para el contexto mecanicista. La evidencia converge en seis procesos que amplifican el riesgo dentro de las horas posteriores a comer: alteración de la señalización de la insulina, eliminación tardía de los lípidos dietéticos, estrés mitocondrial y oxidativo, pérdida de óxido nítrico endotelial, inflamación mediada por el inflamatorio y interacciones microbioma-hormona. Los marcadores dinámicos después de la comida y los compuestos simples como el índice triglicérido-glucosa superan las medidas de ayuno para identificar riesgos y guiar la atención. Las estrategias prácticas para acortar la «ventana de daño» incluyen comidas al estilo mediterráneo con bajos intercambios de índice glucémico y grasas insaturadas, distribución temprana de energía diaria y alimentación temprana restringida por el tiempo, una pequeña porción de proteína antes de la comida y caminata breve después de la comida. Medicamentos de acción rápida: agonistas del receptor insulinotrópico tipo péptido 1 y polipeptídeo dependiente de la glucosa, análogos de la insulina de acción rápida, inhibidores del cotransportador de sodio-glucosa 2 tomados antes de las comidas e inhibidores de la convertasa proproteica subtilisina/kexina de tipo 9; otros picos bruscos, mientras que el monitoreo continuo de la glucosa con retroalimentación algorítmica permite ajustes específicos para cada persona y conscientes del tiempo. Un flujo de trabajo escalonado-pantalla, estratificación y personalización-reestructura la prevención y el tratamiento en torno a la fisiología después de las comidas, con particular relevancia para entornos donde los recursos son limitados. Accede al artículo completo aquí
Suelos contaminados con metales pesados y riesgo de cáncer gástrico: perspectivas moleculares y la relevancia de una perspectiva sanitaria única

Encuentra más información en nuestro repositorio digital La contaminación por metales pesados en los suelos agrícolas ha surgido como un problema crítico de salud pública y ambiental asociado con una mayor incidencia de cáncer gástrico en todo el mundo. Entre los contaminantes más preocupantes están el cadmio, el arsénico y el plomo, que persisten en el medio ambiente y entran al cuerpo humano principalmente a través de la cadena suelo-planta-alimento. Esta revisión integra evidencia ambiental, molecular y epidemiológica para explicar cómo estos metales alteran la biología de la mucosa gástrica y promueven la carcinogénesis. Mecánicamente, el cadmio, el arsénico y el plomo desencadenan estrés oxidativo, disfunción mitocondrial, daño del ADN y reprogramación epigenética, lo que resulta en inestabilidad genómica, resistencia a la muerte celular programada y la transformación de las células epiteliales en fenotipos invasivos. Estas disrupciones moleculares interactúan con la infección por Helicobacter pylori, el desequilibrio microbiano, la inflamación crónica y la remodelación del estroma gástrico inducida por hipoxia, todo lo cual mejora la angiogénesis y la progresión tumoral. Mecánicamente, el cadmio, el arsénico y el plomo desencadenan estrés oxidativo, disfunción mitocondrial, daño del ADN y reprogramación epigenética, lo que resulta en inestabilidad genómica, resistencia a la muerte celular programada y la transformación de las células epiteliales en fenotipos invasivos. Estas disrupciones moleculares interactúan con la infección por Helicobacter pylori, el desequilibrio microbiano, la inflamación crónica y la remodelación del estroma gástrico inducida por hipoxia, todo lo cual mejora la angiogénesis y la progresión tumoral. Fortalecer este enfoque interdisciplinario es esencial para diseñar estrategias preventivas, guiar políticas de remediación y proteger la salud humana, animal y ambiental. Accede al artículo completo aquí
Diversidad genética de Mycoplasma bovis aislado de enfermedad respiratoria bovina y mastitis bovina en Chile
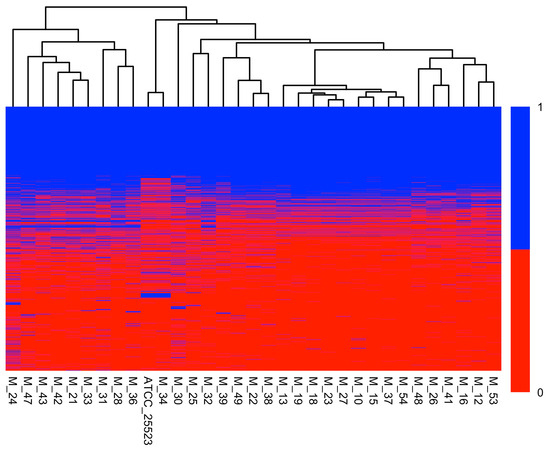
Encuentra más información en nuestro repositorio digital Mycoplasma bovis, un importante patógeno bacteriano para el ganado, es responsable de enfermedades como la neumonía, mastitis, otitis y artritis, lo que lleva a pérdidas económicas sustanciales y preocupaciones por el bienestar animal. A pesar de su amplia distribución global, hay información limitada en América del Sur. M. bovis ha sido reportado como un agente de mastitis en Chile, pero su diversidad genética es poco entendida. Por lo tanto, este estudio tuvo como objetivo determinar la diversidad genética de M. bovis aislados de ganado lechero chileno (en casos de enfermedad respiratoria bovina y mastitis) en las últimas dos décadas y evaluar su relación genética con cepas aisladas en diferentes países utilizando un enfoque de secuenciación del genoma completo. Se encontró que la población de M. bovis en Chile era altamente homogénea, con análisis MLST y filogenómico identificando a ST60 como el clon dominante, representando la mayoría de los aislados (97,8 %), mientras que solo un aislado fue identificado como ST12 (2,2 %). El análisis filogenómico reveló una estrecha relación genética entre la mayoría de los aislados chilenos, mostrando una estrecha relación genética con cepas norteamericanas, formando un clado estrecho con las cepas canadienses ST60, mientras que la única cepa chilena ST12 se agrupaba con norteamericana. Cepas israelíes y europeas agrupadas con la cepa tipo (PG45) de esta especie. Además, el análisis del pangenoma confirma que M. bovis tiene un pangenoma abierto, con una amplia gama de genes accesorios que siguen siendo en gran medida inexplorados y pueden contener ideas clave sobre su plasticidad genómica, abriendo así la investigación futura. Los hallazgos de este estudio proporcionan las primeras perspectivas sobre la estructura poblacional chilena de M. bovis, contribuyendo a la epidemiología global de este patógeno con un enfoque en América del Sur. Estos resultados también abren futuras investigaciones enfocadas en la caracterización integral de este clon dominante, inspirando a la comunidad científica para una mayor exploración de la diversidad genética de M. bovis en Chile. Accede al artículo completo aquí

